18 апреля 2026
Вы здесь
В клиниках и лабораториях. Релизактивность. Современный взгляд на гомеопатию и негомеопатию.
В предлагаемом читателю эссе приведены данные, которые позволяют с позиции современных знаний взглянуть на проблему «малых доз», продемонстрировать перспективы их использования, а также приподнять занавес таинственности, покрывающий гомеопатию.
Более 20 лет я и мои коллеги – научные сотрудники научнопроизводственной фирмы «Материа Медика» совместно с ведущими научноисследовательскими центрами нашей страны посвятили комплексному углублённому, не имеющему аналогов изучению возможностей процесса многократного разведения исходного вещества, впервые применённого основоположником гомеопатии С.Ганеманом и названного им потенцированием. Проведено около 350 экспериментальных исследований с участием лабораторий из 17 стран, несколько десятков клинических исследований, в том числе международных. Полученные результаты позволили прийти к выводу, что технология потенцирования открывает перед современной наукой и техникой новые возможности.
Мы впервые установили, что внешне простая процедура последовательного многократного уменьшения концентрации веществ является сложной технологией, продукты которой приобретают уникальные позитивные свойства. Исторически продукты технологии потенцирования называют «малыми дозами», «гомеопатическими дозами», «потенцированными препаратами», «высокими разведениями». Как мы покажем ниже, эти термины не совсем корректны, но мы будем пользоваться ими как устоявшимися словосочетаниями. Для потенцированных препаратов вместо дозировки указываются шкала разведения (С – сотенная, D – десятичная) и степень разведения; в разведениях выше С12 или D24 в соответствии с числом Авогадро молекулы исходного вещества уже не должны содержаться.
В 1995–1998 гг. мы провели серию экспериментальных и клинических исследований, по окончании которых смогли сформировать современный научный подход к проблеме «малых доз». Для исследований был предложен парадоксальный алгоритм, приведший к парадоксальному результату. Животным одновременно вводили «обычную» – терапевтическую или токсическую дозу известного фармакологического препарата и «малую дозу» этого же препарата (см. таблицу).
Примеры модификации фармакологических эффектов «малыми дозами» препаратов
|
Метод исследования |
Оцениваемый параметр |
Эффект при введении |
|
Диклофенак |
||
|
Тест отдёргивания хвоста |
Латентное время болевой реакции |
Увеличение латентного времени болевой реакции |
|
Модель «уксусные корчи» |
Количество корчей |
Сокращение числа корчей |
|
Тест Гаффнера |
Выраженность болевой реакции |
Уменьшение выраженности болевой реакции |
|
Тест «Открытое поле» |
Пробег, стойки, норки, выходы в центр, умывания, дефекации, уринации |
Снижение выраженности побочных эффектов диклофенака |
|
Интактные животные + токсическая доза диклофенака |
Смертность, динамика массы тела, изменения в поведении |
Укорочение времени реабилитации и уменьшение снижения массы тела |
|
Галоперидол |
||
|
Интактные животные + галоперидол |
Скорость локомоции, мембранный потенциал командных нейронов оборонительного поведения |
Снижение скорости локомоции и гиперполяризация командных нейронов оборонительного поведения |
|
Пароксетин |
||
|
Модели конфликтной ситуации по Vogel |
Число наказуемых взятий воды |
Увеличение числа наказуемых взятий воды как при курсовом, так и при однократном введении |
|
Приподнятый крестообразный лабиринт |
Время нахождения в светлом отсеке, общее число переходов |
Увеличение времени нахождения в светлом отсеке и общего числа переходов как при курсовом, так и при однократном введении |
|
Феназепам |
||
|
Тест «Открытое поле» |
Пробег, стойки, норки, выходы в центр, умывания, дефекации, уринации |
Увеличение двигательной активности крыс |
|
Тест «Вращающийся стержень» |
Число упавших со стержня животных |
Уменьшение числа упавших со стержня животных |
|
Судороги, вызванные коразолом |
Латентный период наступления судорог, доля животных с тоническими судорогами и смертельным исходом |
Увеличение латентного периода наступления судорог, уменьшение количества животных с тоническими судорогами и смертельным исходом |
|
Морфин |
||
|
Абстинентный синдром отмены морфина |
Скорость реакции самостимуляции |
Увеличение функциональной активности и положительной эмоциональной поддержки |
|
Морфинная наркотизация |
Порог ноцицептивной реакции |
Активация антиноцицептивной реакции |
|
Интактные животные + токсическая доза морфина |
Определение летальных доз |
Изменение летальных доз морфина |
|
Интактные животные + морфин |
Потребление кислорода |
Снижение повышенного морфином потребления кислорода |
|
Абстинентный синдром отмены морфина |
Поведение в тесте вынужденного плавания и реакция избегания освещённых мест |
Нормализующий эффект в рамках первого теста и уменьшение предпочтения темноты |
|
Морфинная наркотизация |
Реакция самостимуляции латерального гипоталамуса; поведенческие реакции, характеризующие выраженность абстинентного синдрома |
Повышение частоты самостимуляции латерального гипоталамуса, ослабление реакции активного избегания, усиление реакции замирания на звуковой раздражитель, уменьшение времени развития реакции отдёргивания хвоста |
|
Морфинная наркотизация |
Поведение при применении световых стимулов |
Уменьшение латентного периода реакции на световые стимулы |
|
Изолированные нейроны высших позвоночных |
Электрические параметры изолированных нейронов |
Изменение электрических параметров изолированных нейронов |
|
Этанол |
||
|
Алкоголизация |
Концентрация этанола, активность алкогольдегидрогеназы, определение содержания биогенных моноаминов |
Предупреждение активации этанолом симпатикоадреналовой системы и замедление элиминации этанола из крови |
|
Преднизолон |
||
|
Модель «уксусные корчи» |
Количество корчей и время их наступления, количество экссудата |
Уменьшение количества корчей |
|
Модель артрита, вызванного адъювантом Фрейнда |
Масса отёка, оценка гемограммы |
Уменьшение прироста отёка |
Было установлено, что «малая доза» модифицирует воздействие фармакологического препарата на организм, что обычно проявлялось усилением основного терапевтического действия препарата и одновременно уменьшением его токсичности (в 1997–1998 гг. мы успешно провели клинические исследования препаратов на основе «малых доз» для дезинтоксикации, но отказались от разработки этого направления, а также от разработки препаратов, содержащих «большую» и «малую» дозы одновременно, ради создания препаратов на основе высоких разведений антител). В единичных случаях повышение активности сопровождалось незначительным усилением токсичности. На рисунках 15 приведены наиболее яркие примеры модифицирующего действия «малых доз».
Полученные результаты позволили сделать несколько важных выводов:
1. По своим свойствам «малые дозы» не идентичны исходному веществу, а следовательно, являются отдельным, «самостным» материальным объектом и, возможно, со временем физики смогут определить их природу. Поскольку эффекты «высоких разведений» не могут быть обусловлены молекулами исходного вещества, мы предположили, что носителем свойств «малых доз» является обособленный (дискретный) супрамолекулярный материальный фактор. Об этом косвенно свидетельствует выявленная нами зависимость эффекта «потенцированных препаратов» от «дозы» (степени разведения, условий приготовления, объёма разведений или количества таблеток, частоты назначения) (рис. 6, 7 и 18А).
Более того, в «высоких разведениях» содержится ограниченное количество предполагаемого супрамолекулярного фактора. На примере диклофенака с использованием иммуноферментного анализа (ИФА) (рис. 8) мы показали, что «малая доза» диклофенака способна изменять взаимодействие со своими антителами не всех молекул диклофенака в иммуноферментной реакции, а только их определённой части.
2. Общим уникальным свойством «малых доз» является способность воздействовать на исходное вещество, модифицируя его биологические и физикохимические характеристики (образно говоря, «малая доза» превращается в катализатор (модификатор) действия исходного вещества). Данное свойство носит крайне важный для использования в фармакологии сугубо специфический (специфичность проявляется в том, что действие любого «высокого разведения» направлено только на исходное вещество или его биологические мишени в организме, структурно схожие с исходным веществом) характер; является техногенным и не зависит от наличия молекул в препарате. Приготовленные в процессе потенцирования «высокие разведения», как содержащие детектируемые количества молекул исходного вещества, так и не содержащие их, обладают модифицирующим действием, что подчёркивает роль потенцирования в происхождении «модифицирующего» феномена.
Понятие «доза» подразумевает часть вещества, имеющую те же свойства, что и исходное вещество. «Малые дозы» обладают отличными от исходного вещества особыми свойствами, и, по сути, дозами не являются. Чтобы подчеркнуть техногенное происхождение активности «высоких разведений», мы предлагаем использовать термин «релизактивные препараты» (РАпрепараты), то есть препараты с активностью, высвободившейся в результате процесса приготовления «высоких разведений» исходного вещества.
3. Специфический характер модифицирующих свойств однозначно свидетельствует о том, что в присутствии основного препарата его РАформа воздействует на те же мишени, сенситизирует их и подготавливает к взаимодействию с основным препаратом. Например, РАдиклофенак значимо усиливает ингибирующее воздействие диклофенака в «обычных» дозах на его мишень – циклооксигеназу (рис. 9).
Поскольку с 1998 г. мы преимущественно изучаем РАантитела, на их примере мы установили основные молекулярные механизмы «высоких разведений». Далее мы покажем, что «высокие разведения» способны вызывать тонкие конформационные изменения в молекулахмишенях, что сопровождается изменением характера взаимодействия лигандов с мишенями и включает цепочку молекулярных событий, обусловливающих действие «малых доз».
Открытие основного – модифицирующего действия РАразведений позволило с позиции современных знаний:
оценить исторический опыт применения «малых доз» (экспериментальное изучение биологических эффектов; использование в гомеопатии);
предложить новое – современное таргетное (направленное на биологические мишени) использование продуктов технологии потенцирования.
Исторический опыт применения «малых доз»
Начиная с 1920х годов фармакологи и биологи выявили большое количество биологических эффектов «малых доз» (рис. 10). В России наибольшую популярность получили работы одного из основоположников советской фармакологии академика Н.Кравкова, выдающегося физиолога академика И.Ашмарина и прежде всего профессора Е.Бурлаковой, которой была установлена полимодальная зависимость эффектов потенцированных препаратов от степени разведения и показано, что «малые дозы» воспроизводят лишь часть биологического спектра «обычных» доз.
Действие «малых доз» оказалось плохо воспроизводимым. В своё время скандальную известность получила история с публикацией в журнале «Nature» результатов эксперимента Ж.Бенвениста, которому удалось «высокими разведениями» антител к IgE вызвать дегрануляцию базофилов, но при проверке эффект не был воспроизведён, в итоге журнал «Nature» опубликовал опровержение.
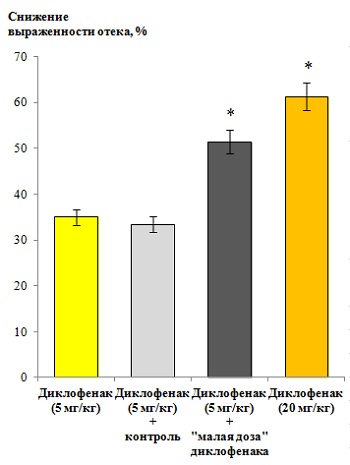
Рис. 1. Оценка способности «малой дозы» диклофенака влиять на противовоспалительную активность диклофенака.
Исследование проводили на модели каррагенининдуцированного воспаления у крыс Вистар. Животные за 60 минут до индукции отёка каррагенином получали внутрижелудочно раствор диклофенака (5 и 20 мг/кг) или его комбинацию (5 мг/кг) с «малой дозой» диклофенака или контролем. Противовоспалительный эффект исследуемых препаратов оценивали через 2 часа после индукции отёка в процентном отношении, исходя из данных массы лап до и после введения каррагенина. *p<0,05 по сравнению с крысами, получавшими диклофенак (5 мг/кг) + контроль.
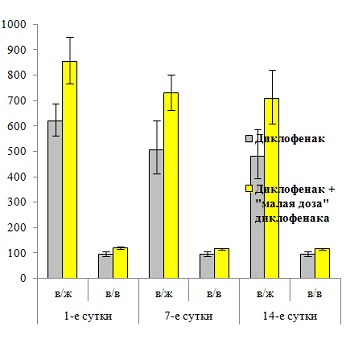
Рис. 2. Оценка способности «малой дозы» диклофенака снижать токсичность диклофенака.
Исследование проводили на модели острой токсичности диклофенака на белых половозрелых крысах. Животные получали однократно внутрижелудочно (в/ж; 5001000 мг/кг) или внутривенно (в/в; 70130 мг/кг) диклофенака, растворённого или в дистиллированной воде, или в водном растворе «малой дозы» диклофенака. Способность «малой дозы» диклофенака снижать токсичность диклофенака оценивали через 14 суток после введения препаратов, рассчитывая показатель ЛД50 (средняя смертельная доза).
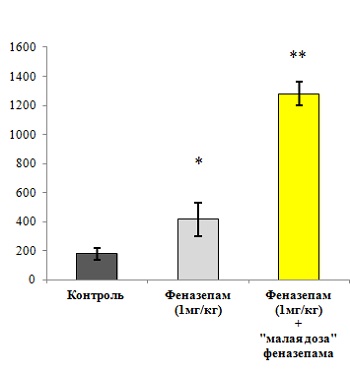
Рис. 3. Оценка способности «малой дозы» феназепама влиять на анксиолитическую активность феназепама.
Исследование проводили на модели конфликтной ситуации по Vogel на беспородных крысах. Животные за 20 минут до начала измерений получали дистиллированную воду (контроль), феназепам (1 мг/кг) или комбинацию феназепама (1 мг/кг) и «малой дозы» феназепама. Анксиолитическую активность оценивали по числу наказуемых взятий воды. *p<0,05; **p<0,01 по сравнению с контролем.

Рис. 4. Оценка способности «малой дозы» галоперидола влиять на тяжесть каталепсии, вызванной введением галоперидола.
Исследование проводили на модели каталепсии на беспородных крысах. Для моделирования состояния каталепсии внутрибрюшинно (за 60 минут до начала наблюдения) вводили раствор галоперидола в дозе 0,07 мг/кг. «Малые дозы» галоперидола вводили одновременно с галоперидолом. Тяжесть каталепсии оценивали по 6балльной шкале по способности животного сохранять искусственно приданную позу на протяжении времени. *p<0,05 по сравнению с крысами, получавшими 0,07 мг/кг галоперидола.
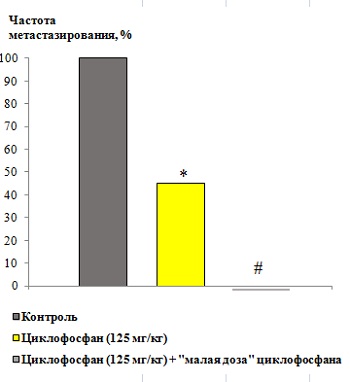
Рис. 5. Оценка способности «малой дозы» циклофосфана влиять на противоопухолевую активность циклофосфана.
Исследование проводили на модели карциномы лёгких Льюис на мышах с перевиваемыми опухолями. Циклофосфан вводили однократно внутрибрюшинно в дозе 125 мг/кг через 1013 суток после трансплантации опухолевых клеток. В опытных группах животные получали «малые дозы» циклофосфана внутрибрюшинно спустя 1 час после инъекции циклофосфана и в течение 810 суток. В контрольных группах животные получали растворитель в соответствующем режиме. Эффективность влияния на частоту метастазирования опухоли (в процентах от общего числа животных в группе) оценивали на 1923е сутки. *p<0,05 по сравнению с контролем; #p<0,05 по сравнению с мышами, получавшими 125 мг/кг циклофосфана.
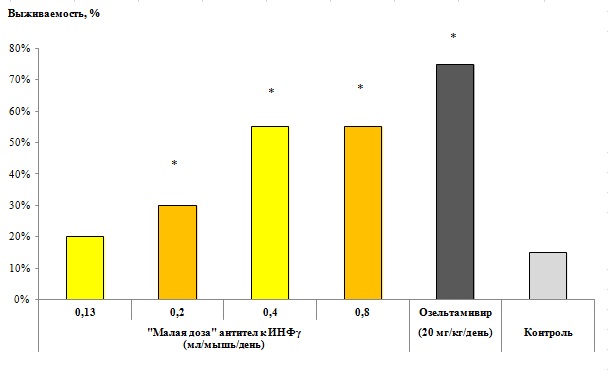
Рис. 6. Дозозависимость противовирусного эффекта «малых доз» антител к интерферону.
Исследование проводили на модели летальной гриппозной инфекции на мышах линии BALB/c, заражённых 10 LD50 вируса гриппа A/California/07/09 (H1N1). Мыши получали «малую дозу» антител к интерферонуγ (ИФНγ) или контроль внутрижелудочно в разных объёмах в течение 5 суток до и 21 суток после инфицирования, а также в свободном доступе с питьём. Животные контрольной группы получали осельтамивир (20 мг/кг в сутки) за 24 часа и 1 час до инфицирования и в течение 5 суток после инфицирования. Гибель животных оценивали дважды в день в течение 3 недель после инфицирования. *p<0,05 по сравнению с контролем.
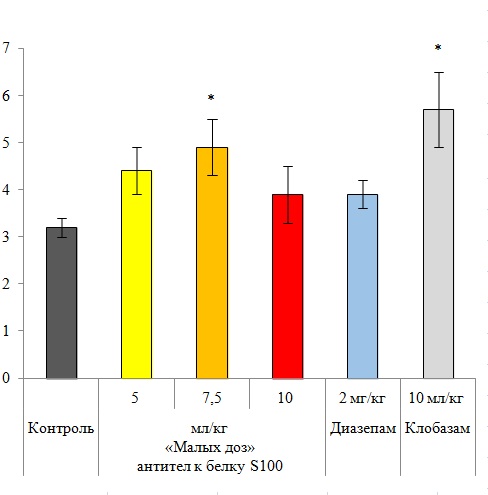
Рис. 7. Дозозависимость анксиолитического эффекта «малых доз» антител к белку S100.
Исследование проводили на модели конфликтной ситуации по Vogel на крысах линии Rj: Вистар (Han). Животные в течение 4 суток получали внутрижелудочно «малые дозы» антител к белку S100, контроль, диазепам (2 мг/кг) или подкожно клобазам (64 мг/кг). Последнее введение – на 5е сутки за 1 час до тестирования. Анксиолитическое действие препаратов оценивали по количеству наказуемых взятий воды из поилок. *p<0,05 по сравнению с контролем.
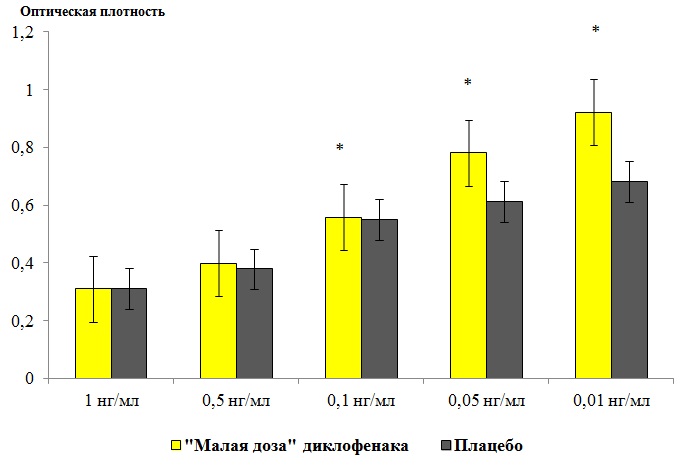
Рис. 8. Оценка способности «малых доз» диклофенака влиять на эффективность взаимодействия диклофенака с антителами.
Исследование проводили методом ИФА с использованием кроличьих поликлональных антител к диклофенаку. Перед проведением ИФА кроличьи поликлональные антитела к диклофенаку предварительно инкубировали с «малой дозой» диклофенака или контролем в соотношении 1 : 2 (v/v) в течение 1 часа. Затем проводили конкурентный ИФА: 100 мкл каждого из преинкубированных растворов антител с образцами и 100 мкл раствора диклофенака в различных концентрациях добавляли в лунки планшета, покрытые конъюгатом диклофенаковальбумин (0,1 мг/мл), после чего следовали стандартному протоколу проведения ИФА. По изменению оптической плотности оценивали влияние «малых доз» диклофенака на количество образовавшихся комплексов «антитела к диклофенакудиклофенак». *p<0,01 по сравнению с контролем.
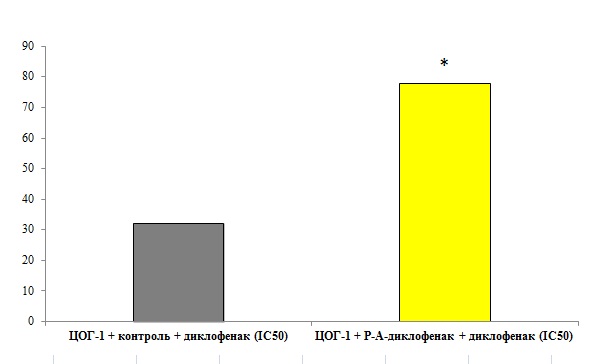
Рис. 9. Оценка способности РАдиклофенака влиять на ингибирующую активность диклофенака в отношении циклооксигеназы1.
Исследование проводили колориметрическим методом. Циклооксигеназу–1 (ЦОГ–1) преинкубировали с РАдиклофенаком, или с контролем в течение 1 часа при комнатной температуре с последующей инкубацией с диклофенаком (IC50) в течение ещё 5 минут. Затем добавляли колориметрический субстрат и арахидоновую кислоту, измеряли оптическую плотность при 590 нм. *p<0,05 по сравнению с группой «ЦОГ–1 + контроль + диклофенак (IC50)».
А Б
Рис. 10. Некоторые примеры опыта применения «малых доз».
А: рисунок адаптирован из работы Н.Кравкова (1924). Б: рисунок адаптирован из работы E.Davenas и соавт. (1988).
Наши результаты объясняют плохую воспроизводимость эффектов «малых доз»: в большинстве случаев исследователи изучали не основное, связанное с сенситизацией биологических мишеней действие «высоких разведений», а вторичные, ускользающие эффекты. Проблема воспроизводимости действия «малых доз» решается, если их исследование проводить «на фоне» обычной дозы, то есть изучать модифицирующее влияние «высоких разведений» на биологическое действие исходного вещества.
Полученные нами результаты, понимание того, что потенцированные препараты, вероятно, содержат супрамолекулярные детерминанты – носители активности, с учётом современных знаний об индивидуальных реакциях позволяют также рассмотреть в новом ракурсе проблему гомеопатии. На сегодняшний день известны как клинические варианты индивидуальных реакций (крапивница, отёк Квинке, анафилактический шок), так и экспериментальные модели реакций гиперчувствительности замедленного, немедленного типа и др. Эти реакции обладают одной общей особенностью – являются неспецифическими (единообразными). Например, отёк Квинке может вызвать любое из известных лекарственных средств, сотни аллергенов вызывают ограниченное число аллергических реакций.
Анализ опыта гомеопатии (главные выводы)
Предложивший гомеопатию С.Ганеман, по сути, является основоположником клинических испытаний лекарственных средств. Он впервые за всю историю медицины целенаправленно проводил исследование лекарственных препаратов в «высоких разведениях» на здоровых добровольцах и обнаружил, что в некоторых случаях они вызывают индивидуальные реакции, воспроизводящие в редуцированном виде картину интоксикации этим же препаратом в «большой» дозе.
Таким образом, в отличие от типовых индивидуальных реакций на лекарственные препараты в «обычных» дозах, имеющих цель заблокировать взаимодействие организма с молекулойантигеном, на менее опасный для организма супрамолекулярный фактор – носитель релизактивности – организм отвечает специфически.
На основании проведённых клинических исследований С.Ганеман предложил два терапевтических приёма, составляющих основу гомеопатии:
1. Симптомы, выявленные при испытании препарата на здоровых, использовать как симптомымишени при лечении больных (принцип подобия, от греческого óμοιος – «подобный»).
2. Назначать гомеопатические препараты только больным с высокой индивидуальной чувствительностью к ним – в соответствии с фенотипическими маркёрами, которые С.Ганеман выявлял у «респондентов» на тот или иной гомеопатический препарат в ходе клинической апробации на здоровых добровольцах. Таким образом, цель гомеопатического назначения – вызвать «малой дозой» индивидуальную реакцию у пациента.
Исследования биологической активности «малых доз», проведённые нашими предшественниками – биологами, и наши собственные исследования показывают, что «высокие разведения» всегда вызывают молекулярноклеточные реакции.
Мы впервые выявили, что при направленном (таргетном) применении выраженность физиологического действия РАпрепаратов достаточна для оказания терапевтического действия и создания на основе «малых доз» лекарственных препаратов.
В дофармакологическую эру С.Ганеман, не зная о биологических особенностях «высоких разведений», предложил, по сути, единственную для своего времени возможность применения «малых доз», усиливая физиологическое действие «малых доз» через иммунологические механизмы индивидуальной чувствительности и вызывая индивидуальные реакции.
В связи с этим С.Ганеману и его последователям удавалось достичь терапевтического действия только в тех случаях, когда у больных с высокой индивидуальной чувствительностью нормальная физиологическая реакция на гомеопатический препарат на молекулярном уровне трансформируется в атипичный системный, целостный (холистический) ответ на уровне всего организма, вызывая позитивную перестройку его регуляции. В гомеопатии действует принцип «всё или ничего», встречающийся в иммунологии. Поэтому терапевтическая эффективность действия гомеопатических препаратов никогда не сможет быть доказана в рамках современных стандартных клинических исследований на однородной популяции больных; гомеопатия априори не может быть частью доказательной медицины. Любое «высокое разведение» обладает «потенциальной энергией», которую врачгомеопат должен суметь целенаправленно филигранно использовать. Эффективность гомеопатической терапии полностью зависит от профессионализма врачагомеопата, которому необходимо овладеть колоссальным объёмом знаний в виде описания действия нескольких тысяч гомеопатических препаратов. Даже опытным гомеопатам далеко не всегда на первом приёме удаётся определить «подходящий» данному больному препарат, что значимо ограничивает возможности этого метода.
С учётом того, что биология и её часть, медицина, принадлежат к естественным наукам, объектами их изучения являются закономерности живой Природы, то есть повторяющиеся, воспроизводимые события, поддающиеся статистической обработке. Поскольку индивидуальная реакция не может быть воспроизведена на всей популяции, в данном аспекте гомеопатия является врачебным искусством, донаучным эмпирическим методом лечения. В отличие от доказанных эффектов фармакологических препаратов любой гомеопатический препарат можно рассматривать как шанс на выздоровление – при условии, что врачгомеопат сумеет вызвать у пациента позитивный индивидуальный ответ на назначенный препарат. Гомеопатическую терапию не следует противопоставлять современной медицине; гомеопатия может прекрасно дополнять общепринятую фармакотерапию, особенно при лечении хронических заболеваний.
Современное применение препаратов на основе «малых доз»
Гомеопатия – явный терапевтический прорыв для своего времени, но, конечно, она не может решать задачи гарантированного лечения, которые общество сегодня ставит перед медициной. Однако современные знания о тонких механизмах биологической регуляции организма позволяют использовать технологию потенцирования для создания эффективных инновационных препаратов.
В ходе нашей исследовательской работы мы обнаружили ранее неизвестное специфическое модифицирующее действие «малых доз», что открывает возможности для их направленного (таргетного) – фармакологического применения; доказали, что на основе «малых доз» регуляторных молекул могут быть созданы эффективные и безопасные биологические препараты.
Фармакологическое и гомеопатическое применение «малых доз» базируется на принципиально разных биологических механизмах. В первом случае выявляют и используют физиологическое действие «высоких разведений», во втором – их атипичные гиперергические индивидуальные реакции.
Вследствие этого фармакологические препараты в «малых дозах» должны соответствовать общим требованиям, предъявляемым к современным лекарственным средствам, и прежде всего проходить клинические испытания в соответствии с правилами доказательной медицины. Гомеопатические препараты, напротив, должны подвергаться гомеопатическому прувингу – исследованию на здоровых добровольцах с целью выявления клинических симптомов индивидуальных реакций.
Для того чтобы различать фармакологическое и индивидуальное применение препаратов, произведённых методом потенцирования, мы предлагаем для первых использовать термин «релизактивные» препараты, а для вторых – «гомеопатические».
Нами заложены базовые основы фармакологии РАпрепаратов на примере антител. Антитела были выбраны в качестве перспективных фармакологических агентов после того, как в 1998 г. под руководством академика М.Штарка на известной нейробиологической модели длительной посттетанической потенциации неожиданно было установлено, что «малые дозы» антител не подавляют активность молекулантигенов, а модифицируют её, то есть оказывают сонаправленное с антигеном действие (рис. 11).
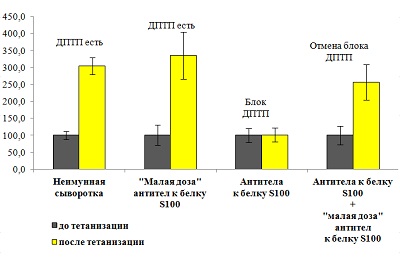
Рис. 11. Модифицирующая активность «малых доз» антител к белку S100.
Исследование проводили на поперечных срезах гиппокампа половозрелых крыс. Срезы помещали в камеру с проточной средой Ямамото, аэрируемой карбогеном, и инкубировали в течение 40 минут, затем регистрировали возбуждающие постсинаптические потенциалы (ВПСП). Для этого стимулирующий электрод помещали в область мшистых волокон, а регистрирующий стеклянный электрод – в область САЗ в зоне начальных сегментов апикальных дендритов. После выработки длительной посттетанической потенциации (ДПТП) к срезам добавляли тестируемые образцы и в течение 20 минут регистрировали ВПСП.
Данное обстоятельство существенно расширяет терапевтический потенциал антител, которые в современной фармакологии используются преимущественно в онкологии с целью подавления активности тех или иных молекул, участвующих в канцерогенезе. В «высоких разведениях» антитела могут применяться при лечении широкого круга соматических заболеваний.
Антитело представляет собой иммуноглобулин со сложной биохимической структурой, синтезируемый плазмоцитами – потомками βлимфоцитов, который присутствует в сыворотке крови и других биологических жидкостях и предназначен для связывания молекулантигенов. Связывание обеспечивается особенным строением антител (рис. 12).
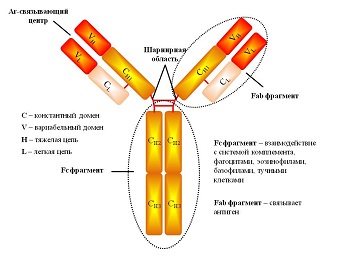
Рис. 12. Строение иммуноглобулина G.
Иммуноглобулины содержат 2 вида парных полипептидных цепей: лёгкие (L, от англ. light – лёгкий), с низкой молекулярной массой, и тяжёлые (H, от англ. heavy – тяжёлый), с высокой молекулярной массой. Все 4 цепи соединены вместе дисульфидными связями. Каждая цепь представлена двумя внеклеточными иммуноглобулиноподобными доменами (вариабельным на NHконце и константным), стабилизированными при помощи SSсвязей, и цитоплазматическим стабильным COOHконцом. Nконцевые области L– и Нцепей (Vобласть) образуют 2 антигенсвязывающих центра – (Fab)2фрагмент. Fcфрагмент молекулы взаимодействует со своим рецептором на мембране различных типов клеток (макрофаги, нейтрофилы, тучные клетки).
Вследствие уникальной структуры антител присущее всем «малым дозам» свойство целенаправленно воздействовать на исходное вещество (или его мишени в организме, структурно схожие с исходным веществом) заметно усилилось, когда мы начали использовать «малые дозы» антител.
Наиболее изученным в ходе экспериментальных исследований препаратом в «малых дозах» на данный момент является Анаферон, содержащий РАантитела к интерферонуγ (ИФНγ). На его примере с использованием спектроскопии ядерномагнитного резонанса (ЯМР) установлены фундаментальные механизмы действия «малых доз» – способность изменять конформационные характеристики мишеней (в данном случае ИФНγ), что приводит к «включению» физиологического ответа на введение в организм «малой дозы».
Как видно на рисунке 13, препарат изменяет конформационное состояние молекулы ИФНγ. Как мы продемонстрировали, эти изменения конформации молекулымишени (ИФНγ) лежат в основе всех последующих молекулярноклеточных событий: в увеличении количества молекул ИФНγ, связавшихся с рецептором (рис. 14), и, как следствие, в повышении экспрессии эндогенного ИФНγ (рис. 15), то есть приводят к активации сигнального пути ИФНγ.
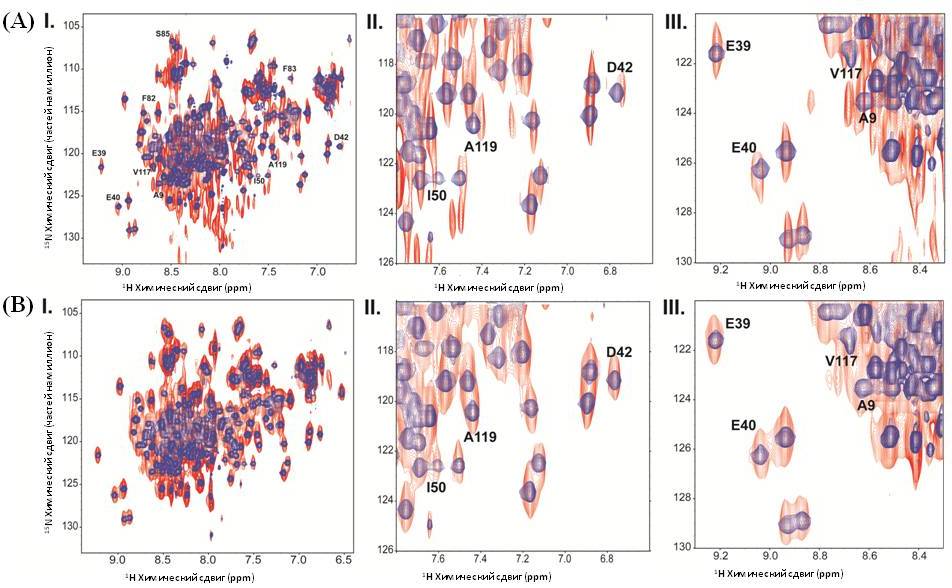
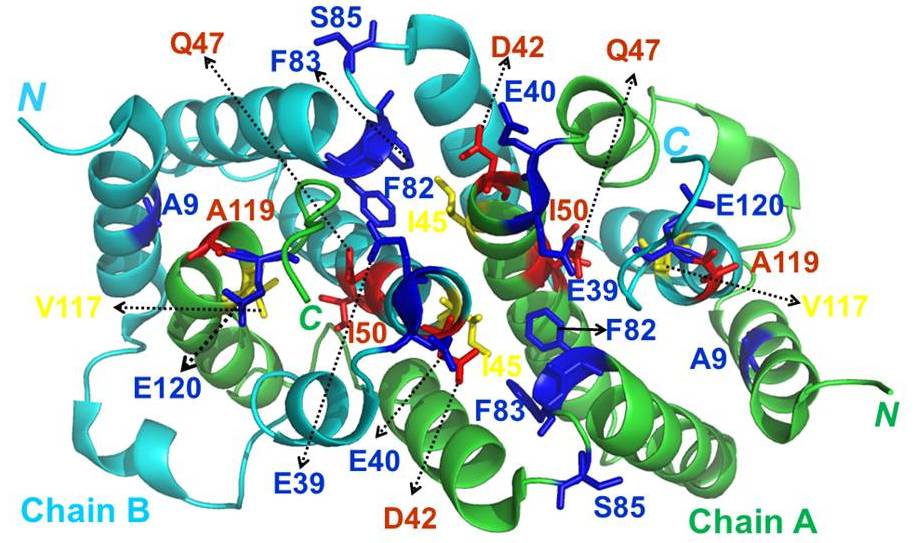
Рис. 13. Влияние РАантител к ИФНγ на конформационное состояние молекулы ИФН.
Исследование проводили методом спектроскопии ЯМР. РАантитела к ИФНγ или плацебо добавляли к 15Nмеченному ИФНγ. Спектры были получены с помощью стандартной последовательности импульсов HSQC в 2048 сканах в протонном измерении и 34 сканах в азотном измерении с задержкой в секунду. Наблюдаемые основные резонансы устанавливались на основании ранее опубликованных данных ЯМР, полученных при аналогичных условиях для ИФНγ. Наверху: 15N1HHSQCспектры ИФНγ в отсутствие (синий цвет) и в присутствии (красный цвет) РАантител к ИФНγ (A) или плацебо (B). По осям абсцисс – 1Hхимический сдвиг (ppm), по осям ординат – 15Nхимический сдвиг (ppm). Полноразмерные спектры (с 6,5 до 9,5 ppm) показаны на (I). Спектры двух участков, содержащих сильно пертурбированные сигналы, увеличены и показаны на (II) и (III).
Справа: картирование изменений химического сдвига, наблюдаемых в 15N1HHSQCспектре 15Nмеченного ИФНγ после добавления РАантител к ИФНγ.
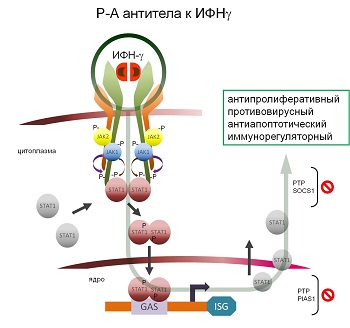
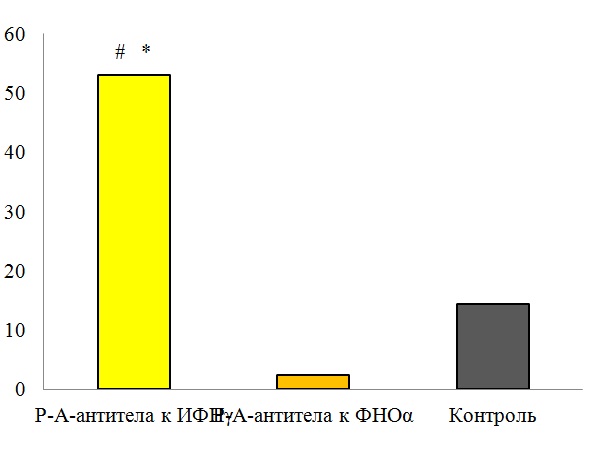
Рис. 14. Влияние РАантител к ИФНγ на связывание молекулы ИФНγ со своим рецептором.
Слева: исследование проводили с использованием моноцитов U937 методом радиолигандного анализа. Для оценки общего связывания к клеткам добавляли тестируемые образцы, радиолиганд [125I]ИФНγ; инкубировали 150 минут; центрифугировали; отбирали супернатант, отмывая от взвеси клеток, и регистрировали радиоактивность в течение 1 минуты с помощью счётчика излучения. Показатели специфического связывания радиолиганда с рецептором ИФНγ рассчитывали как разность между общим и неспецифическим связыванием (измеренным в присутствии избытка немеченного ИФНγ). * p<0,05 по сравнению с контролем #p<0,05 по сравнению с группой «РАантитела к фактору некроза опухоли α (ФНО α)». Справа: схематичное изображение сигнального пути ИФНγ.
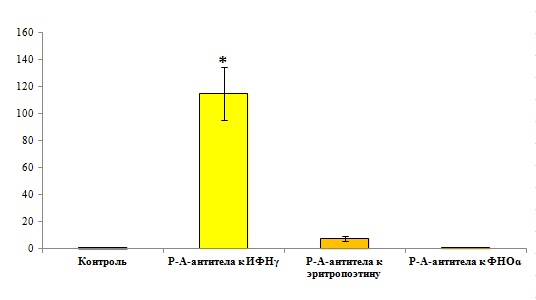
Рис. 15. Влияние РАантител к ИФНγ на продукцию клетками ИФНγ.
Исследование проводили на мышах линии CBA/CaLac. Тестируемые образцы вводили перорально в течение 10 суток. На 4е сутки после введения выделяли лимфоциты из взвеси селезёночных клеток мышей. Количество жизнеспособных лимфоцитов доводили до концентрации 2 х 106 клеток/мл и инкубировали в полной культуральной среде в течение суток. Концентрацию ИФНγ в культуральных средах определяли с использованием ИФА. *p<0,05 по сравнению с контролем.
На основе «малых доз» можно создавать не только средства, предназначенные для лечения соматических заболеваний, но и препараты с психотропной активностью. После того, как в 1998 г. мы открыли необычные модифицирующие свойства «высоких разведений» антител с использованием антисыворотки к белку S100, антитела к этому белку в «малых дозах» были подвергнуты углублённому экспериментальному изучению, а на его основе был создан препарат Тенотен. В основе механизмов Тенотена лежит модификация физиологического действия нейроспецифического белка S100.
На рисунках 16-18 в качестве примера приведены результаты исследования анксиолитической, антидепрессивной и нейропротективной активности Тенотена, а также механизмы его действия.
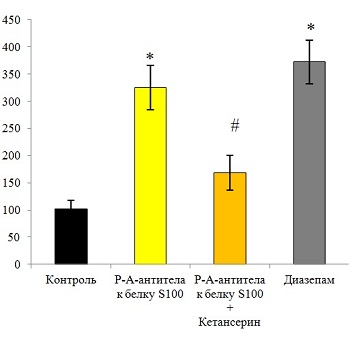
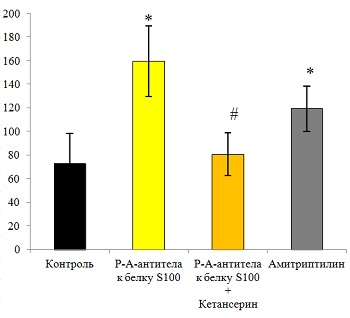
Рис. 16. Результаты исследования анксиолитической и антидепрессивной активности РАантител к белку S100.
Исследование проводили на модели конфликтной ситуации по Vogel (А) и модели вынужденного плавания по Nomura (Б) на беспородных белых крысах. Животные за 20 минут до тестирования получали внутрижелудочно контроль; РАантитела к белку S100; внутрибрюшинно кетансерин (избирательный антагонист 5НТ2/5НТ1С рецепторов, 1 мг/кг) и через 10 минут РАантитела к белку S100; препарат сравнения диазепам (2 мг/кг) или амитриптилин (15 мг/кг). Анксиолитический и антидепрессивный эффект исследуемых препаратов оценивали по количеству наказуемых взятий воды (А) и по количеству оборотов колёс (Б), которые животные делают в попытке выбраться из сосуда, заполненного водой, соответственно. *p<0,05 по сравнению с контролем, #p<0,05 по сравнению с группой, получавшей РАантитела к белку S100.
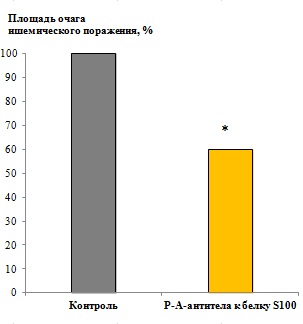
Рис. 17. Результаты исследования нейропротективной активности РАантител к белку S100.
Исследование проводили на модели ишемии головного мозга крыс Вистар. Перед введением тестируемых препаратов животным моделировали двусторонний фокальный ишемический очаг в префронтальной коре головного мозга с помощью метода фотохимического тромбоза. Контроль или РАантитела к белку S100 вводили внутрижелудочно в течение 9 суток после моделирования ишемического инсульта. Нейропротективную активность исследуемых препаратов оценивали, исходя из площади очага поражения до и после введения препаратов. *p<0,05 по сравнению с контролем.
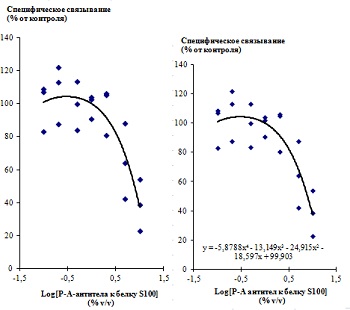
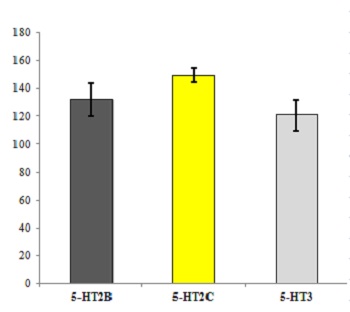
Рис. 18. Результаты исследования вовлечённости сигма1рецептора (А) и серотониновых (Б) рецепторов в механизм действия РАантител к белку S100.
Исследование влияния РАантител к белку S100 на связывание стандартных радиолигандов: [3H](+)пентазоцин для сигма1рецептора (А), [3H]ЛСД для 5HT2B рецептора, [3H]–месулергин для 5HT2C, [3H]BRL43694 для 5HT3 (Б) in vitro проводили с использованием клеток Jurkat (сигма1рецептор) или CHOK1 (рецепторы серотонинергической системы). Для оценки общего связывания гомогенаты мембран клеток вносили в лунку вместе с контролем или исследуемым препаратом; добавляли соответствующие радиолиганды; смесь инкубировали, пропускали через фильтры и промывали охлаждённым буфером. Фильтры высушивали и измеряли радиоактивность на сцинтилляционном счётчике. Неспецифическое связывание измеряли аналогичным образом, но вместо препарата или контроля в лунку добавляли немеченый лиганд (галоперидол (10 мкM) для сигма1рецептора; ритансерин (1 мкМ), 5гидрокситриптамин (100 мкМ) или MDL72222 (100 мкМ) для 5HT2B, 5HT2С и 5HT3 рецепторов соответственно). Показатели специфического связывания радиолиганда с соответствующим рецептором рассчитывали как разность между общим и неспецифическим связыванием. Результаты выражали в процентах от специфического связывания в контроле.
Экспериментальное изучение «малых доз», включая все необходимые токсикологические тесты и фундаментальное изучение молекулярных механизмов действия, явилось первым шагом к созданию на основе антител нового класса лекарственных препаратов, разработчики которого были отмечены премией Правительства РФ за 2005 г.; в 2006 г. премией Правительства РФ за разработку препарата Тенотен была удостоена группа молодых учёных.
Отличительной особенностью препаратов данного класса является то, что вместо той или иной регуляторной молекулы (эритропоэтин, ИФН-γ, инсулин и т.д.) в организм вводится модификатор взаимодействия этой молекулы с её биологической мишенью в виде «высоких разведений» поликлональных антител к этой молекуле или к её рецептору.
Поскольку для препаратов в «малых дозах» не существует биологических барьеров, а значит – и проблемы биодоступности, главным преимуществом РАантител является способность специфически воздействовать на любую молекулумишень в организме. Например, препарат, содержащий «малые дозы» антител к βсубъединице рецептора инсулина, специфически воздействует на свою мишень – внутриклеточный домен рецептора инсулина, что приводит к активации сопряжённого с инсулиновым рецептором сигнального пути, вызывая повышение продукции адипонектина (рис. 19).

Рис. 19. Специфичность действия РАантител к βсубъединице рецептора инсулина.
Исследование проводили на зрелых адипоцитах человека. Клетки человека инкубировали в течение 3 суток в присутствии тестируемых образцов. Оценивали способность комбинированного препарата, содержащего РАантитела к βсубъединице рецептора инсулина (ИР) и РАантитела к эндотелиальной NOсинтазе (eNOS), в отсутствие инсулина влиять на секрецию адипонектина. Уровень секреции адипонектина в питательной среде измеряли с использованием ИФА. *p<0,001 по сравнению с другими группами.
Также важным достоинством препаратов на основе «малых доз» является их нормализующее, адаптивное действие. Например, препарат, содержащий РАантитела к эритропоэтину, нормализует уровень эритропоэтина как в случае его повышения, так и в случае снижения относительно нормы (рис. 20).
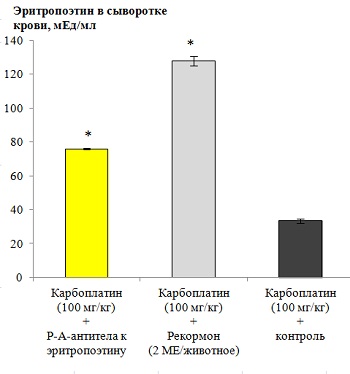
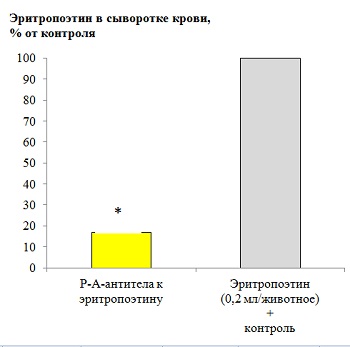
Рис. 20. Нормализующее действие РАантител к эритропоэтину.
А: Исследование проводили на модели миелосупрессии у мышей линии CBA/CaLac. Патологию вызывали однократным внутрибрюшинным введением 100 мг/кг карбоплатина. За 5 суток до введения карбоплатина и в течение 10 суток после животные получали внутрижелудочно РАантитела к эритропоэтину или контроль. Содержание эритропоэтина в сыворотке крови определяли с помощью ИФА. *p<0,05 по сравнению с мышами, получавшими карбоплатин (100 мг/кг) + контроль.
Б: Исследование проводили на модели иммобилизационного стресса у мышей линии CBA/CaLac. Животные в течение 10 суток после 10часовой иммобилизации получали внутрижелудочно РАантитела к эритропоэтину или контроль. Содержание эритропоэтина в сыворотке крови определяли с помощью ИФА. *p<0,05 по сравнению с мышами, получавшими эритропоэтин (0,2 мл/животное) + контроль.
Препараты в «малых дозах» практически не имеют токсичности, мы не наблюдали случаев пристрастия и привыкания к ним.
Следующим шагом к созданию нового класса лекарственных препаратов явилось проведение рандомизированных клинических исследований (РКИ) в соответствии с принципами доказательной медицины. Возможность таргетного воздействия на ключевые патологические процессы при конкретной нозологии была использована для разработки инновационных средств для лечения гриппа и острых респираторных вирусных инфекций, ожирения и сахарного диабета 1го и 2го типа, тревожных расстройств, синдрома раздражённого кишечника, ВИЧинфекции и др.
Только за последние несколько лет с разрешения Минздрава России и регуляторов других стран проведено более 30 РКИ с участием около 7 тыс. пациентов, из которых около 3 тыс. – дети, начиная с возраста 1 месяц. Пострегистрационный опыт применения препаратов включает значительно большее число участников независимых (инициативных) исследований.
В РКИ принимали и принимают участие ведущие медицинские и научноисследовательские центры России, стран СНГ, а также некоторых стран дальнего зарубежья.
В ходе РКИ, проведённых в соответствии с правилами Надлежащей клинической практики, было прежде всего показано, что, в отличие от казуальной гомеопатии, эффективность современных фармакологических препаратов на основе «малых доз» может быть установлена в ходе классических клинических испытаний, и они могут соответствовать канонам доказательной медицины.
В качестве примера клинической эффективности РАпрепаратов на основе поликлональных антител приводим краткое резюме клинических исследований комплексного трёхкомпонентного препарата Эргоферон для лечения гриппа и острых респираторных вирусных инфекций.
В связи с тем, что в состав препарата входят РАантитела к СD4рецептору лимфоцитов, он оказывает влияние на клеточное звено иммунитета. За последние несколько лет в клинических исследованиях препарата Эргоферон уже приняли участие 2028 пациентов. К настоящему времени завершён анализ трёх многоцентровых РКИ с участием 1067 пациентов, в том числе 306 детей, в ходе которых методом двойного слепого плацебоконтроля доказана эффективность Эргоферона в лечении острых респираторных вирусных инфекций. В многоцентровом сравнительном РКИ с применением дизайна «Noninferiority» показана сопоставимость терапевтической эффективности Эргоферона и осельтамивира/Тамифлю® у взрослых пациентов с сезонным гриппом А и В. Результаты данного РКИ размещены на сайте ClinicalTrials.gov и опубликованы в научном рецензируемом журнале Международного общества по инфекционным заболеваниям – «International Journal of Infectious Diseases».
Таким образом, экспериментально и клинически мы доказали, что фармакологическое действие «малых доз» воспроизводимо и сопоставимо по эффективности с действием «обычных» лекарственных средств тех же фармакотерапевтических групп; при этом они не вызывают серьёзных нежелательных реакций.
Полученные результаты и прежде всего данные по клинической апробации были представлены в ходе научных консультаций в ведущих мировых медицинских агентствах – Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA), Европейское агентство лекарственных средств (EMA, Европа) и Агентство по регулированию лекарственных средств и продуктов для здравоохранения (MHRA, Великобритания). В результате анализа и обсуждения мы везде получили заключение, что препараты на основе РАантител не являются гомеопатическими, а относятся к биологическим препаратам. В качестве примера приводим выдержку из документа Ref: 1029/Anaferon от 28 сентября 2015 г. по результатам научных консультаций с экспертами MHRA (Великобритания): «Анаферон не должен регистрироваться в соответствии с государственными требованиями Великобритании к гомеопатическим препаратам, поскольку в настоящее время препарат находится вне рамок британских гомеопатических традиций по указанным показаниям. Анаферон считается биологическим препаратом и подлежит полной процедуре регистрации лекарственного средства. Поскольку это противовирусный лекарственный препарат, то Централизованная процедура – единственный способ регистрации препарата Анаферон».
В России на сегодняшний день указанные препараты также не относятся к гомеопатическим. Мы проводим большую работу по международной унификации требований к инновационным препаратам, созданным нашей фирмой, и утверждению для них единой терминологии.
Наконец, мы сделали следующий очень важный шаг к созданию нового класса лекарственных средств – разработали принципы детекции релизактивности.
Много лет назад мы установили, что основное модифицирующее действие «малых доз» воспроизводится вне организма. Например, с помощью «высоких разведений» мы изменяли скорость химических реакций (рис. 21) и физикохимические свойства исходных веществ.
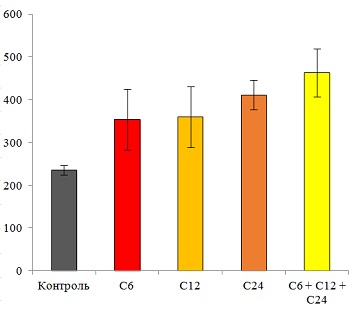
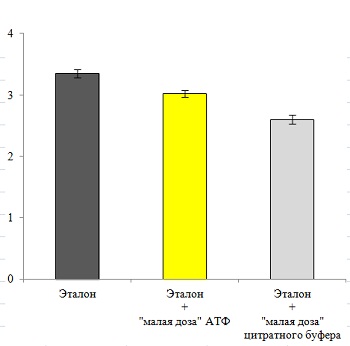
Рис. 21. Модифицирующая активность «малых доз» веществ, оценённая по скорости протекания химических реакций.
А: Исследование проводили на Фурьеспектрометре в условиях термостатирования с регистрацией спектров ЯМР 31Р. Эталон представлял собой раствор из динатриевой соли аденозинтрифосфата (АТФ) (0,02 моль/л), моногидрата лимонной кислоты (0,08 моль/л), гидроксида натрия, дейтерированной (10% об.) и дистиллированной воды. Для получения экспериментальных образцов в данную смесь добавляли «малые дозы» АТФ (10% об.) или «малые дозы» цитратного буфера (10% об.).
Б: Исследование проводили с использованием метода переменнотоковой инверсионной вольтамперометрии для фиксации низких концентраций солей Hg (II). К образцам «малой дозы» Hg(NO3)2 в разведениях С6, С12, С24, С6+С12+С24 добавляли 1 мл 1М раствора LiCl и 1 мл бидистиллированной воды. В качестве контроля использовали 1М раствор LiCl. После перемешивания накапливали ртуть на стеклоуглеродном рабочем электроде в течение 99 секунд. Данные представлены в виде величины площади под графиками сигналов, вычисленных из вольтамперометрической кривой.
Возможность изучать модифицирующее действие «малых доз» вне организма позволяет разрабатывать аналитические методики их определения и, кроме того, в будущем, возможно, позволит физикам, с которыми мы активно сотрудничаем, приблизиться к пониманию физической природы релизактивности.
За последние десятилетия накоплены данные многих исследований с применением различных физикохимических методов (например, кондуктометрия, pHметрия, вискозиметрия, калориметрия, люминисцентная спектроскопия, спектрофотометрия в УФ и видимой областях, флуоресцентная микроскопия, атомносиловая микроскопия, ИКспектроскопия, КРспектроскопия, ЯМРрелаксометрия, детекция электромагнитного сигнала, исследование кристаллогенезиса, метод кристаллизации капель, ЯМРспектроскопия, анализ диэлектрических свойств, атомноэмиссионная спектрометрия и массспектрометрия). Большинство из упомянутых методов показывают, что «высокие разведения» различных веществ обладают структурированностью, в том числе и «высокие разведения» антител.
Мы также апробировали многие из упомянутых методик и в итоге пришли к выводу, что наше открытие наилучшим образом подходит и для детекции «малых доз» в готовых лекарственных формах: определение должно основываться на их базисном свойстве – модифицирующей активности (рис. 22, 23).
Например, с применением ИФА можно изучать влияние препарата Анаферон на изменение связывания ИФН с антителами, что позволяет определять модифицирующую активность препарата (рис. 22).
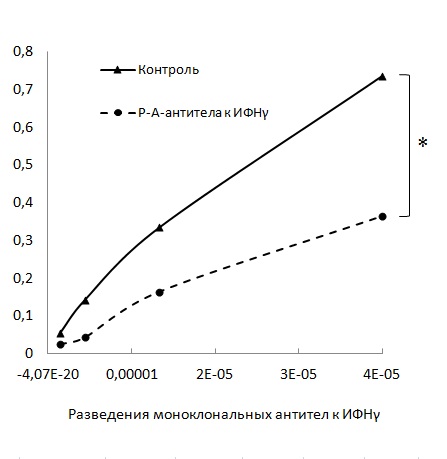
Рис. 22. Определение модифицирующей активности РАантител к ИФНγ методом ИФА.
Исследование проводили с использованием растворов моноклональных антител к ИФНγ в концентрациях 7200 нг/мл. Растворы моноклональных антител к ИФНγ инкубировали с РАантителами к ИФНγ или контролем в соотношении 1 : 4 (v/v) в течение 45 минут. Затем преинкубированные растворы добавляли в лунки планшета с адсорбированным ИФНγ в концентрации 0,7 мкг/мл. Далее проводили ИФА по стандартному протоколу с измерением оптической плотности при длине волны 490 нм. *p<0,0001 по сравнению с контролем.
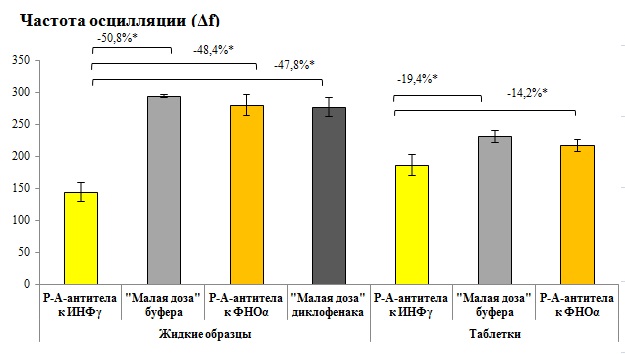
Рис. 23. Определение модифицирующей активности РАантител к ИФНγ методом пьезокварцевых иммуносенсоров.
Исследование проводили методом пьезокварцевых иммуносенсоров с использованием образцов в жидкой лекарственной форме, а также предварительно растворённых таблеток. Тестируемые образцы смешивали с раствором ИФНγ в соотношении 4 : 1 (v/v) и инкубировали в течение часа. Затем анализируемые пробы в потоке раствораносителя в проточноинжекционном режиме пропускали над поверхностью пьезокварцевых иммуносенсоров с иммобилизованными на их поверхности антителами к ИФНγ (2,4 нг/мл). Регистрировали аналитический сигнал сенсора (изменение частоты осцилляции пьезокварцевого резонатора), пропорциональный массе образованного поверхностного иммунокомплекса. Активность РАантител к ИФНγ оценивали через величину изменения аналитического сигнала по сравнению с остальными протестированными образцами – контроль («малая доза» буфера) и контролями специфичности. *p<0,05 по сравнению с указанными группами.
Из изложенного следует, что нам удалось решить многие вопросы внедрения препаратов на основе «высоких разведений» в современную медицину, что сопровождалось и сопровождается многими сложностями.
Технические сложности обусловлены прежде всего тем, что на сегодняшний день физики не сумели объяснить природу «малых доз», они являются объектаминевидимками. Мы измеряем релизактивность, но не знаем её носителя. Однако перспективы применения модифицирующих свойств «высоких разведений» в науке и технике настолько велики, что этот пока нерешённый вопрос не должен останавливать исследователей.
Нашу работу постоянно сопровождают и идеологические сложности. Исторически общие – модифицирующие свойства «высоких разведений» были открыты в 1996 г. – в год 200летия опубликования С.Ганеманом принципов гомеопатии. Таким образом, общие свойства «малых доз» стали известны через 200 лет после открытия частного свойства «малых доз» – способности вызывать индивидуальные специфические гиперергические реакции, лежащей в основе гомеопатической терапии.
В течение всего периода своего существования гомеопатия вызывает критическое отношение к себе, так как для любого здравомыслящего человека отсутствие молекул в гомеопатических препаратах и недоказанность гомеопатии в клинических исследованиях являются весомыми аргументами против реальности её существования. Надо признаться, что и автор этих строк, имея классическое медицинское образование, также в своё время относился к гомеопатии с недоверием – до того момента, пока лично не столкнулся со случаями клинической эффективности гомеопатической терапии. Проведённые нами исследования, если и не решают всех вопросов, связанных с малыми дозами и гомеопатией в частности, то позволяют определить место релизактивных разведений в современной системе биологических знаний.
Наибольшей заслугой основателя гомеопатии С.Ганемана является не столько сама гомеопатическая терапия, сколько предложенная им внешне простая и до сих пор неоценённая технология градуального уменьшения концентрации веществ. Способность продуктов данной технологии прицельно воздействовать на исходное вещество и модифицировать его свойства, обязательно со временем будет востребована и в медицине, и в химии, и в технике.
Мы продолжаем искать для технологии потенцирования разные направления применения. В данное время нами подготовлены к проведению клинической апробации крайне перспективный препарат для преодоления резистентности к антибиотикам; препараты, обладающие высокой эффективностью при лечении таких тяжёлых заболеваний, как последствия инсульта, ДЦП, аутизм и другие нервнопсихические расстройства; биологические препараты для ветеринарии.
В своей работе мы периодически сталкиваемся с тем, что нигилизм к гомеопатии распространяется и на РАпрепараты. Например, нам через Высокий суд Лондона пришлось получать патенты на наши препараты в Великобритании, так как патентное ведомство этой страны традиционно негативно настроено к гомеопатии и поэтому критично отнеслось к предоставленным нами сведениям о РАпрепаратах, ошибочно посчитав их гомеопатическими.
«Малые дозы», как любое необъяснимое явление, часто вызывают психологическую защиту в виде отторжения. Поэтому мы особо ценим каждый случай мудрого, широкого подхода к «непознанному».
Данное эссе я позволю себе завершить выдержкой из личного письма, которое в 1998 г. я получил от известного физика, лауреата Нобелевской премии, основателя комиссии по лженауке Российской академии наук В.Гинзбурга. Виталий Лазаревич высказал мнение о моей первой публикации, посвящённой экспериментам с «малыми дозами», выпущенной в виде брошюры. В письме приведены несколько серьёзных критических замечаний, которые я полностью учёл в своей дальнейшей работе, а заканчивается оно следующими словами: «В заключение хочу поделиться с Вами некоторыми замечаниями, касающимися гомеопатии. Я не понимал (и сейчас не до конца понимаю), как могут существовать две медицины: аллопатия и гомеопатия. Ведь нет же двух математик или физик. В медицине же имеются аллопаты, гомеопаты и народные целители (я не говорю о шарлатанах). Всё дело, очевидно, в сложности человеческого организма и его болезней и одновременно недостаточной развитости медицины. Но, думаю, недалеко то время, когда медицина впитает в себя всё положительное, что есть в гомеопатии».
Смею надеяться, что внедрение в современную доказательную медицину технологии потенцирования полностью соответствует этим словам.
Олег ЭПШТЕЙН,
доктор медицинских наук,
членкорреспондент РАН,
лауреат премии Правительства РФ
в области науки и техники.
- Войдите или зарегистрируйтесь, чтобы отправлять комментарии

Издательский отдел: +7 (495) 608-85-44 Реклама: +7 (495) 608-85-44,
E-mail: mg-podpiska@mail.ru Е-mail rekmedic@mgzt.ru
Отдел информации Справки: 8 (495) 608-86-95
E-mail: inform@mgzt.ru E-mail: mggazeta@mgzt.ru





